[국내연구자 소개] 김기진 교수/차의과대학 생명과학대학
관리자
view : 2839

- 김기진 교수 (gjkim@cha.ac.kr)
차의과학대학교 생명과학대학 의생명과학과, 태반연구실
I. 연구실 개요
- 제 연구실은 차의과학대학교 생명과학대학 의생명과학과 소속으로, 2006년 9월부터 현재까지 인간 태반을 구성하는 주요 세포인 영양막세포의 기능 분석, 인간 태반의 발달 및 발달이상에 따른 산과질환, 그리고 태반유래 중간엽줄기세포의 특징과 만성 간질환, 안과질환, 난소기능부전, 난임 등 다양한 퇴행성 질환 동물 모델에서의 태반유래 중간엽줄기세포 (placenta-derived mesenchymal stem cells, PD-MSCs)의 치료 효능과 그 치료 기전을 규명할 뿐 아니라, 태반내 유효성분을 추출하여 활용 가능성 연구 등 인간 태반 조직을 기반으로, 태반연구를 진행하고 있는 국내 유일한 태반연구실 (Placenta Research Laboratory, PRL) 입니다.
특히, 줄기세포 기반 진행중인 프로젝트로는 다양한 만성 간질환 동물 모델에서 이식된 태반유래 중간엽줄기세포의 치료 효능을 분석한 결과, CCl4, TAA 등과 같이 화학물 혹은 담관절제술 (Bile duct ligation, BDL) 등에 의해 유도된 만성 간경변증 동물에서 염증성 사이토카인 발현이 감소되는 반면, 항염증성 사이토카인은 증가되어 염증이 완화되고, 간 조직내 축적된 섬유화가 감소될 뿐 아니라, 세포자살 현상이 억제되면서, 자가포식 (autophagy)이 증가되면서, 손상받은 간세포의 증식이 증가되면서 간세포의 재생능이 향상되는 것을 보고하였다.
또한, 갑상선 호르몬 이상으로 인한 갑상샘 안질환 동물모델에서 이식된 태반유래 중간엽줄기세포는 염증을 완화시킬 뿐 아니라 시신경의 재생을 유도할 뿐 아니라 갑상샘 안질환의 병인학적 요인인 비정상적인 adipogenesis 관련 유전자들의 발현을 조절시킴으로써, 지방 축적을 억제한다는 결과를 보고하였다.
난소절제술과 cyclophosphamide/busulfan, 그리고 TAA 등으로 유도된 난소기능부전 동물 모델에 이식된 태반유래 중간엽줄기세포는 손상된 난소 조직내에서의 염증반응을 낮추는 반면, 난포형성조절 인자들의 발현을 증가시켜 난포의 성숙과 발달에 관여하는 것을 확인하였음. 특히, 이식한 태반유래 중간엽줄기세포에 의해 난포의 형성과 성숙이 진행되면서 관련된 호르몬 에스트로겐 (E2)과 AMH 등 호르몬의 증가가 관찰되었음. 이러한 난소의 기능 개선은 현재까지 호르몬 치료에 의존적인 난임 치료법의 한계를 극복할 수 있는 생식의학 분야의 새로운 치료제 개발로 연계될 가능성이 높아 최근 연구가 활발히 진행되고 있는 상황임.
난소의 기능 개선 뿐 아니라 난임의 근본적인 원인 중 하나는 정상적으로 수정된 배아의 자궁 내착상이 원할하게 이루어지지 않는 부분인데, 특히, 착상 단계에서 수정된 배아의 외층에 존재하고 있는 영양막세포의 침윤능이 정상적으로 작동하지 않아 자궁내막에 착상을 하지 못해 난임을 초래한다. 따라서, 이러한 영양막세포의 침윤능을 향상시킬 수 있는 것이 생식의학 분야에서의 최대관심사이다. 흥미롭게도 영양막세포의 in vitro 배양을 태반유래 중간엽줄기세포와 공배양을 유도하였을 때, 영양막세포의 MMPs 발현과 활성도가 증가되면서, 영양막세포의 침윤능이 증가되는 것을 보고하면서, 이러한 영양막세포의 침윤능 증가에도 태반유래 중간엽줄기세포 기반 치료제 개발이 가능하다고 사료된다.
이처럼, 태반연구실에서는 태반유래 중간엽줄기세포를 기반으로, 현재까지 치료법이 제한적인 다양한 퇴행성 질환 및 난치성 질환에 적용하고, 그 치료 효능과 기전을 규명하고 있다.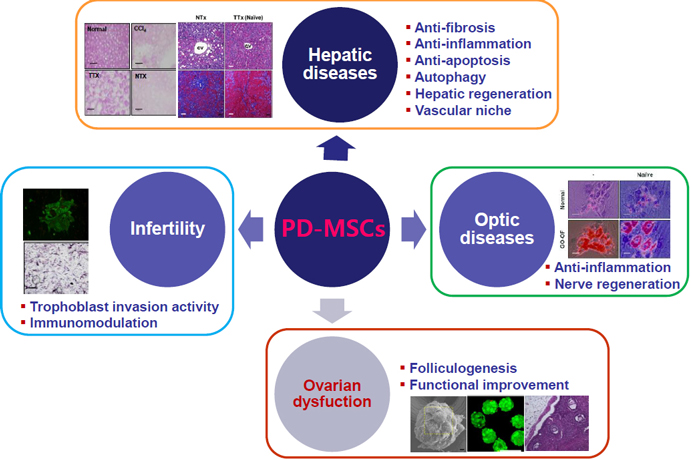
그림. 태반연구실내 현재 진행중인 태반유래 중간엽줄기세포 치료제 개발 프로젝트
II. 연구 배경 및 주요 연구내용
- 1) 만성 간질환 세포치료제 개발 프로젝트
-
태반연구실에서는 지난 2006년부터 태반유래 중간엽줄기세포를 이용한 다양한 만성 간질환 동물 모델에서의 치료효능 및 그 치료 기전에 대한 연구를 진행해 왔다. 간경변증은 현재까지 적절한 치료법이 없는 만성 퇴행성 질환으로, 이 질환 기간이 지속되면 결국 간암으로까지 진행할 수 있는 비가역적인 질환으로, 간부전으로 인한 간이식 이외에는 특별한 치료법이 없는 실정이다. 제한된 간이식 기회와 그에 따른 비용적 의료적 부적용으로 인해 새로운 치료법 개발이 시급한 질환이다. 이러한 상황에서, 태반유래 중간엽줄기세포의 분리, 배양, 특징 분석 및 분화능을 기반으로, 태반유래 중간엽줄기세포의 면역조절능 등을 보고하였으며, 이러한 태반유래 중간엽줄기세포를 사염화탄소 (CCl4) 또는 담관절제술에 의해 제작된 간손상 동물 모델에 이식 후, 이식한 줄기세포의 정착율과 이식 경로에 따른 간경변증 동물모델에서의 치료효능을 다각적인 방법으로 분석 보고하였다. 특히, 이식한 태반유래 중간엽줄기세포는 염증반응을 현저히 억제시키고, 섬유화된 간 조직에서의 콜라젠 축적을 억제하는 항섬유화능이 관찰되었으며, 이식한 줄기세포에 의한 세포사조절 기전을 통해 apoptosis는 억제하면서, autophagy (자가포식) 기전은 활성화 함으로써, 간세포의 증식을 활성화 시키는 것을 확인하였다. 특히, IL-6/STAT3 신호전달 체계를 후성학적 조절 기전인 메틸화를 조절함으로써, 손상된 간세포의 증식을 증가시키는 것을 확인하였다. 또한, 간경변증 동물 모델에서 이식한 태반유래 중간엽줄기세포에 의해 변화된 microRNA 프로파일링을 분석한 결과, Epithelial-Mesenchymal Transition (EMT) 기전을 조절하는 microRNA가 발굴 및 조절 기전을 특징을 분석하였다. 최근에는 이식한 태반유래 중간엽줄기세포에 의해 손상된 간 조직의 재생 기전을 통하여 대사체 분석을 진행함으로써, 간세포의 증식 뿐 아니라 대사기능과 같은 기능적인 재생관련 연구가 활발히 진행되고 있으며, 이러한 치료 효능을 모니터링할 수 있는 인자들의 발굴 및 분석 등에 대한 연구가 활발히 진행되고 있다.
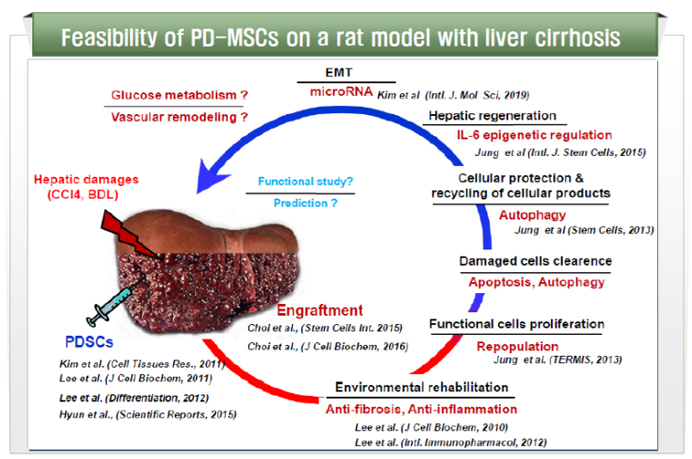
그림. 태반유래 중간엽줄기세포 이식에 따른 간경변증 동물모델에서의 치료 효능 및 조절 기전 - 2) 난소기능부전 세포치료제 개발 프로젝트
-
현재 난소기능부전 치료를 위한 방법으로는 호르몬제재를 이용한 치료가 사용되고 있으나, 약물부작용, 암발현 가능성, 과배란에 의한 부작용 등 다양한 부작용등으로 새로운 치료법이 필요한 상황임 - 줄기세포를 이용한 난소기능 향상 및 난소기능부전 치료의 접근으로 국내, 외에서도 연구가 거의 없는 상황으로 희소성과 독창적인 연구로 본 연구과제의 결과는 국제적으로 줄기세포의 위상을 제고할 수 있다고 생각되어 지고 있음. 특히, 태반유래 중간엽줄기세포를 이용한 난소기능 회복 가능성은 본 연구진의 긍정적인 예비연구결과를 바탕으로 매우 고무적인 것으로, 태반유래 중간엽줄기세포를 이용한 세포치료제가 개발된다면, 난소기능부전의 원인에 상관없이 안전하면서도 비교적 용이한 방법으로 난소 내에 존재하는 원시난포(primordial follicles)의 성장을 시작할 수 있도록 적용 가능할 것으로 기대하고 있다. 특히, 난소기능부전은 난소절제술과 cyclophosphamide/busulfan, 그리고 TAA 등으로 유도된 난소기능부전 동물 모델에 이식된 태반유래 중간엽줄기세포는 손상된 난소 조직 내에서의 염증반응을 낮추는 반면, 난포형성조절 인자들의 발현을 증가시켜 난포의 성숙과 발달에 관여하는 것을 확인하였음. 특히, 이식한 태반유래 중간엽줄기세포에 의해 난포의 형성과 성숙이 진행되면서 관련된 호르몬 에스트로겐 (E2)과 AMH 등 호르몬의 증가가 관찰되었음. 이러한 결과는 지난 2018년 한국줄기세포학회에서 우수 포스터상을 수상하였으며 (2018.08.16), 지난 미국 워싱턴 DC에서 개최된 2019 American Society for Cell Biology (ASCB) 학회에서도 우수 포스터상을 수상하였다 (2019.12.11). 이러한 난소의 기능 개선은 현재까지 호르몬 치료에 의존적인 난임 치료법의 한계를 극복할 수 있는 생식의학 분야의 새로운 치료제 개발로 연계될 가능성이 높아 최근 연구가 활발히 진행되고 있는 상황으로, 현재 공도연구를 진행하고 있는 혁신형 제약회사측으로 기술이전 준비를 통하여 난소기능부전 세포치료제 개발을 위한 준비가 활발히 진행되고 있음.
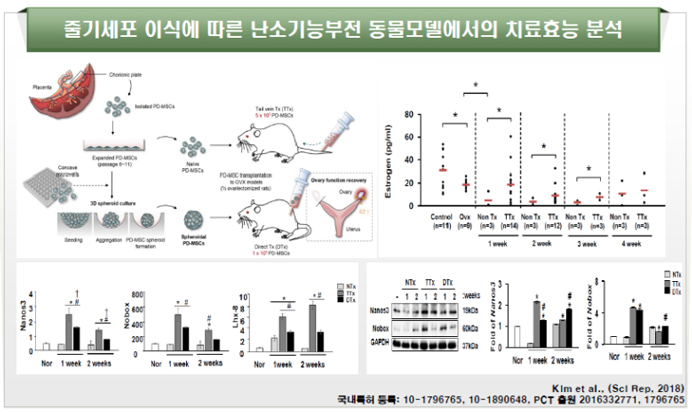
그림. 태반줄기세포 이식에 따른 난소기능부전 동물 모델에서의 치료 효능 및 기전 분석 - 3) 갑상샘 안질환 세포치료제 개발 프로젝트
-
갑상샘안질환은 그 발병 원인 과도한 thyroid 분비로 인한 자가면역질환으로, 안와주변의 섬유아세포의 과도한 지방 축적 및 섬유화로 인한 안구통증 및 시력감소 등 발병율이 점차적으로 증가되고 잇는 만성 희귀질환으로, 현재까지의 치료법은 제한된 스테로이드 치료법이 외에는 적절한 치료법이 없는 질환이다. 특히, 적절한 동물 모델 제작 및 검증 또한 어려운 실정으로, 본 연구팀에서는 thyroid receptor를 인위적으로 고농도로 장기간 동안 투약하여 사람의 갑상샘안질환과 유사하게 제작된 동물 모델에 태반유래 중간엽줄기세포를 이식 후 면역조절능 및 안와주변 조직에서의 지방 축적, 섬유화, 그리고 MRI 등을 이용한 안와주변 조직의 두께 등을 분석한 결과, 태반유래 중간엽줄기세포를 이식한 그룹에서 스테로이드 처방한 그룹과 유사한 염증완화 효능, 지방 축적 억제로 인한 안와조직의 부피 감소, 그리고 섬유화 억제 등에 관련된 치료 효능 결과들을 보고하였으며, 관련 특허를 국내 출원 및 PCT 출원 등을 통하여, 국내 안과전문 제약회사로의 기술이전이 진행 중에 있다.
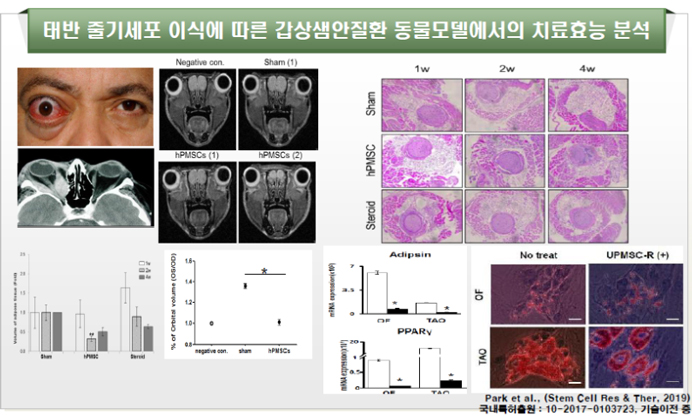
그림. 태반줄기세포 이식에 따른 갑상샘안질환 동물모델에서의 치료효능 및 치료 기전 분석
따라서, 태반연구실에서는 다양한 퇴행성 질환 또는 희귀질환에서의 태반유래 중간엽줄기세포의 치료 효능과 그 기전 (mode of action, MoA)을 분석함으로써, 태반유래 중간엽줄기세포기반 세포치료제 개발관련 프로젝트들을 활발히 진행하고 있다.
III. 관련 논문 (최근 5년간)
- Jun JH, Kim JY, Choi JH, Lim JY, Kim KG, Kim GJ*. Exosomes from placenta-derived mesenchymal stem cells are involved in liver regeneration in hepatic failure induced by bile duct ligation. Stem Cells Intl. 2019 (in press)
- Seok J, Jung HS, Park S, Lee JO, Kim CJ, Kim GJ*. Alteration of fatty acids oxidation by increased CPT1A on replicative senescence of placenta-derived mesenchymal stem cells. Stem Cell Res & Ther 2019 (in press)
- Kim GD, Choi JH, Lim SM, Jun JH, Moon JW, Kim GJ*. Alterations in IL-6/STAT3 Signaling by Korean Mistletoe Lectin Regulate the Self-Renewal Activity of Placenta-Derived Mesenchymal Stem Cells. Nutrients. 2019 Oct 30;11(11).
- Kim JY, Jun JH, Park SY, Yang SW, Bae SH, Kim GJ*. Dynamic Regulation of miRNA Expression by Functionally Enhanced Placental Mesenchymal Stem Cells PromotesHepatic Regeneration in a Rat Model with Bile Duct Ligation. Int J Mol Sci. 2019 Oct 24;20(21).
- Heo JS, Pyo S, Lim JY, Yoon DW, Kim BY, Kim JH, Kim GJ, Lee SG, Kim J. Biological effects of melatonin on human adipose‑derived mesenchymal stem cells. Int J Mol Med. 2019 Dec;44(6):2234-2244.
- Park M, Banga JP, Kim GJ, Kim M, Lew H. Human placenta-derived mesenchymal stem cells ameliorate orbital adipogenesis in female mice models of Graves'ophthalmopathy. Stem Cell Res Ther. 2019 Aug 9;10(1):246.
- Heo JS, Lim JY, Pyo S, Yoon DW, Lee D, Ren WX, Lee SG, Kim GJ*, Kim J. Environmental Benzopyrene Attenuates Stemness of Placenta-Derived Mesenchymal Stem Cells via Aryl Hydrocarbon Receptor. Stem Cells Int. 2019 Jan 13;2019:7414015. (co-corresponding author)
- Kim SH, Jung J, Cho KJ, Choi JH, Lee HS, Kim GJ*, Lee SG. Immunomodulatory Effects of Placenta-derived Mesenchymal Stem Cells on T Cells by Regulation of FoxP3 Expression. Int J Stem Cells. 2018 Nov 30;11(2):196-204. (co-corresponding author)
- Kim TH, Choi JH, Jun Y, Lim SM, Park S, Paek JY, Lee SH, Hwang JY, Kim GJ*. 3D-cultured human placenta-derived mesenchymal stem cell spheroids enhance ovary function by inducing folliculogenesis. Sci Rep. 2018 Oct 17;8(1):15313.
- Kim HW, Lee HS, Kang JM, Bae SH, Kim C, Lee SH, Schwarz J, Kim GJ, Kim JS, Cha DH, Kim J, Chang SW, Lee TH, Moon J. Dual Effects of Human Placenta-Derived Neural Cells on Neuroprotection and the Inhibition of Neuroinflammation in a Rodent Model of Parkinson's Disease. Cell Transplant. 2018 May;27(5):814-830.
- Na JY, Seok J, Park S, Kim JS, Kim GJ*. Effects of selenium on the survival and invasion of trophoblasts. Clin Exp Reprod Med. 2018 Mar;45(1):10-16.
- Lee YB, Choi JH, Kim EN, Seok J, Lee HJ, Yoon JH, Kim GJ*. Human Chorionic Plate-Derived Mesenchymal Stem Cells Restore Hepatic Lipid Metabolism in a Rat Model of Bile Duct Ligation. Stem Cells Int. 2017;2017:5180579.
- Kim SH, Kim GJ*, Umemura T, Lee SG, Cho KJ. (2017) Aberrant expression of plasma microRNA-33a in an atherosclerosis-risk group. Mol Biol Rep. 44(1):79-88. (Co-first author)
- Jun JH, Choi JH, Bae SH, Oh SH, Kim GJ*. (2016) Decreased C-reactive protein induces abnormal vascular structure in a rat model of liver dysfunction induced by bile duct ligation. Clin Mol Hepatol. 22(3):372-381
- Lim SM, Jang HY, Lee JE, Shin JS, Park SH, Yoon BH, Kim GJ*. (2016) Alteration of Pituitary Tumor Transforming Gene-1 Regulates Trophoblast Invasion via the Integrin/Rho-Family Signaling Pathway. PLoS One. 11(2):e0149371.
- Choi JH, Lee YB, Jung J, Hwang SG, Oh IH, Kim GJ*. (2016) Hypoxia Inducible Factor-1α Regulates the Migration of Bone Marrow Mesenchymal Stem Cells via Integrin α 4. Stem Cells Int. 2016:7932185
- Ahn J, Son MK, Jung KH, Kim K, Kim GJ, Lee SH, Hong SS, Park SG. (2016) Aminoacyl-tRNA synthetase interacting multi-functional protein 1 attenuates liver fibrosis by inhibiting TGFβ signaling. Int J Oncol. 48(2):747-55.
- Choi JH, Lim SM, Yoo YI, Jung J, Park JW, Kim GJ*. (2015) Microenvironmental Interaction Between Hypoxia and Endothelial Cells Controls the Migration Ability of Placenta-Derived Mesenchymal Stem Cells via α4 Integrin and Rho Signaling. J Cell Biochem. Oct 8. doi: 10.1002/jcb.25398.
- Hyun J, Wang S, Kim J, Kim GJ, Jung Y. (2015) MicroRNA125b-mediated Hedgehog signaling influences liver regeneration by chorionic plate-derived mesenchymal stem cells. Sci Rep. 15;5:14135.
- Jung J, Moon JW, Choi JH, Lee YW, Park SH, Kim GJ*. (2015) Epigenetic Alterations of IL-6/STAT3 Signaling by Placental Stem Cells Promote Hepatic Regeneration in a Rat Model with CCl4-induced Liver Injury. Int J Stem Cells. 2015 May;8(1):79-89.
- Gong JS, Kim GJ*. (2015) The role of autophagy in the placenta as a regulator of cell death. Clin Exp Reprod Med. 2014 Sep;41(3):97-107.
[등록 특허]- 태반 융모막판유래 중간엽줄기세포의 고순도 분리방법 (등록: 10-0900309)
- 불멸화된 중간엽 줄기세포주의 제조방법 (등록 제10-1892071)
- 태반유래 혈청 대체물의 제조방법 및 이를 이용한 성체줄기세포의 배양방법 (등록 10-1092851)
- 태반유래 줄기세포 또는 태반 추출물을 포함하는 착상 장애로 인한 불임의 예방 또는 치료용 약학조성물 (등록: 10-00858225)
- 태반유래 줄기세포를 포함하는 난소기능부전 혹은 갱년기 증후군의 예방 또는 치료용 약학조성물 (등록 제10-1890648, PCT출원: 10-1796765-0000)

