[임상연구 동향] 조혈모세포 이식 임상연구 동향
관리자
view : 2805
조혈모세포 이식 임상연구 동향
백은정
한양대학교 의과대학 진단검사의학과 부교수
개요
- 조혈모세포이식(hematopoietic stem cell transplantation, HSCT)은 유전성 혈액질환이나, 혈액암 등에 효과적인 치료로서 최근 유전자치료와 함께 그 중요성이 계속 부각되고 있다. 기존의 혈액종양 질환 적응증 외에 다양한 질환에 대해 조혈모세포이식법에 대한 관심이 높아져서 최근 자가 조혈모세포이식을 통해 자가면역질환을 치료하는 사례가 늘고 있다[1].
성공적인 동종조혈모세포의 착상과 기능을 위하여 이식 전처치로 환자의 면역체계를 억제하고 문제 있는 조혈모세포를 제거하는 것이 필요한데, 이를 위해 시행하는 방사선 치료나 항암제로 인한 독성, 불임, 및 사망률 증가 등에 대한 위험이 높아진다. 골수제거 없이 면역억제만으로 동종세포의 착상이 가능하게 하는 강도경감 전처치 방법도 사용되고 있다.
만약 목표하는 줄기세포만 선택적으로 죽일 수 있거나 독성을 낮출 수 있다면, 조혈모세포이식법은 훨씬 더 안전하게 다양한 적응증에 시행될 수 있을 것이다. 본 글에서는 기존의 전형적인 혈액종양 질환에 대한 조혈모세포 이식 외에 다양한 질환에 대한 조혈모세포이식법 도입에 대한 소개와, 화학요법과 방사선치료 없이 자가나 동종 조혈모세포이식이 가능하게 하는 단클론항체 기반 전처치법(conditioning regimen)에 관련한 비임상 및 임상 연구결과들을 소개하고자 한다. - 1) 다발성 경화증 (Multiple Sclerosis)에서 비골수제거 자가 조혈모세포이식(nonmyeloablative autologous HSCT) 치료 연구
- Northwestern 대학의 Richard K. Burt 연구팀은 무작위임상시험을 통해 조혈모세포이식이 현재 disease-modifying therapy (DMT) 치료법보다 재발완화형 다발성 경화증 (Relapsing-Remitting Multiple Sclerosis) 환자에서 질병진행을 억제하는데 효과적이라고 발표하였다. 대상 환자 110명 중 절반은 기존의 약물치료를 받게 했으며 나머지 절반의 환자들은 이식전 처치로 cyclophosphamide와 antithymocyte globulin을 투여하여 비골수제거 자가 조혈모세포이식(nonmyeloablative HSCT)을 받게 했다.
1년 후, 연구팀은 각 환자의 질병이 어느 정도 진행되었는지를 평가에서 1점 이상 악화된 환자의 비율은 약물치료군의 약 25%이지만, 조혈모세포이식군에서는 2%여서 이식군에서 질병 악화를 억제하는 효과가 더 좋음을 발표했다[2]. 그 외 이식받은 환자들에서 여러 증상이나 삶의 질 면에서 더 좋은 효과를 보였다. 연구팀은 앞으로 장기간 임상결과와 안전성에 대해 연구를 진행하겠다고 했다.
2. 전신피부경화증
- 자가면역질환의 하나인 전신피부경화증(systemic scleroderma)환자의 경우에도 비골수제거 자가 조혈모세포이식을 통해 성숙한 면역세포들을 제거하고 자신의 혈액줄기세포를 주입할 경우 면역계의 초기화을 통해 질환의 완화(remission)될 수 있다고 발표하였다[2]. 자가 조혈모세포이식 후 54 개월째에 두 배 이상의 환자들이 기존 cyclophosphamide 치료를 받은 경우에 비해 더 유의하게 좋은 결과를 보였다. 또한, event-free survival 비율도 자가 조혈모세포이식 그룹에서 79%로서 약물치료만 받은 그룹의 50%이 비해 유의하게 높았다. 그러나, 치료로 인한 사망률은 약물치료그룹에 비해 조혈모세포그룹에서 더 높았다[2].
3. 조혈모세포이식의 최신동향: 조혈모세포 표적 공격
- 골수내 조혈모세포만 파괴하여 기존의 조혈모세포이식 과정의 위험도를 낮추는 연구들이 진행되고 있다[3].
미국 캘리포니아의 Forty Seven 회사와 NIH 및 Stanford대 연구팀은 c-Kit (stem cell growth factor receptor) 항체(FSI-174)와 CD47에 대한 항체(magrolimab, 5F9)를 이용해 원숭이를 대상으로 조혈모세포 표적 공격 실험에서 조혈모세포 수를 줄이는 데 성공하였다[4]. c-Kit 조혈모세포에서 발현되며, CD47은 “don’t eat me” signal인데, FSI-174만 사용하거나, magrolimab과 복합사용법에 의해 면역세포에 의한 c-Kit 양성 조혈모세포의 phagocytosis 효과를 높일 수 있다고 보고했다. 이 방법으로 무차별적으로 세포를 손상시키는 기존의 전처치법에 비해 사망률 등의 위험도를 낮추며 이식된 조혈모세포가 효과적으로 생착할 수 있도록 할 것으로 보인다. 앞으로 이런 표적 제거 방법으로 이식될 세포들의 장기 정착을 허용할 수 있을지와 2020년에 계획중인 임상시험에서도 비슷한 효과를 낼지에 대해 추가 연구결과가 기대된다.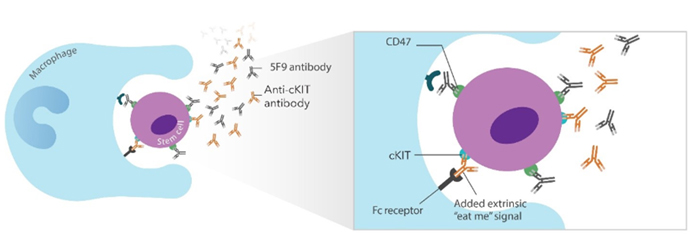
C-KIT Antibody FSI-174 Program by FortySeven
(그림 출처: https://www.fortyseveninc.com/science)
4. c-Kit 항체를 이용한 조혈모세포 표적 공격
- 매사추세츠주의 Magenta Therapeutics 회사와 미국 국립보건원(US National Institutes of Health)의 연구팀과 조혈모세포의 선택적 제거를 위한 연구를 시행했다[5]. c-Kit에 대한 항체를 사용해 조혈모세포의 c-kit과 결합한 후 독소를 분비하여 세포를 살해하게 한다. 생쥐실험과 원숭이 한마리를 이용한 실험에서, 이 항체는 이식전처치 효과가 충분하게 골수 조혈모세포를 죽이지만, 면역세포 등의 다른 세포들은 죽이지 않았다.
다른 치료예로서, 스탠퍼드 대학교의 Judith Shizuru팀과 캘리포니아의 암젠(Amgen) 회사는, 면역계가 손상된 유전적 장애를 가진 아기들을 대상으로 c-Kit를 겨냥하는 항체를 개발했다[3]. 6명의 아기들은 동종 조혈모세포 이식을 받았으며, 네 아기에서 골수이식이 성공한 것으로 발표했다.
5. 결론 및 향후 전망
- 조혈모세포이식의 적응증이 확장되어 가고 있지만 여전히 치료 과정중의 위험요소가 높으므로, 조혈모세포 표적 제거법과 같은 연구가 진척되면 향후 많은 환자들이 더 안전하게 좋은 치료를 받게 될 것이라 생각한다.
References
-
- J.R. Passweg, H. Baldomero, P. Bader, et al., Is the use of unrelated donor transplantation leveling off in Europe? The 2016 European Society for Blood and Marrow Transplant activity survey report, Bone marrow transplantation 53(9) (2018) 1139-1148.
- K.M. Sullivan, E.A. Goldmuntz, L. Keyes-Elstein, et al., Myeloablative Autologous Stem-Cell Transplantation for Severe Scleroderma, The New England journal of medicine 378(1) (2018) 35-47.
- H. Ledford, Targeted stem-cell attack could make transplants safer, Nature, 576 (2019) 18-19.
- Kristopher D Marjon, James Y Chen, Jiaqi Duan, et al., An All Antibody Approach for Conditioning Bone Marrow for Hematopoietic Stem Cell Transplantation with Anti-cKIT and Anti-CD47 in Non-Human Primates, ASH annual meeting, 2019 Abstract No. 4428.
- John F. Tisdale, Robert E. Donahue, Naoya Uchida, et al., A Single Dose of CD117 Antibody Drug Conjugate Enables Autologous Gene-Modified Hematopoietic Stem Cell Transplant (Gene Therapy) in Nonhuman Primates, ASH annual meeting, 2019. Abstract No. 610.
