[임상연구 동향] 체외 생산된 줄기세포 유래 혈액 제제의 임상연구 동향
관리자
view : 3892
작성자: 백은정(한양대학교)
체외 생산된 줄기세포 유래 혈액 제제의 임상연구 동향
- 1. 개요
- 체외 생산된 줄기세포 유래 혈액제제는 바이오의약품 분류 중 세포치료제이기도 하면서 최종 상품은 혈액제제이기도 해서 임상시험시 여러 분류와 항목들의 조정이 필요할 것으로 보인다. 2016년 바이오의약품 국내 시장 규모는 약 1조 8,308억 원이고 이 중 혈액제제(혈장분획제제 제외)는 11% 정도이지만, 국내 혈액가가 일부 선진국의 5분의 1정도 임을 감안하면 시장규모 내 비중이 적지가 않다.
(출처: 한국바이오의약품 협회 식품의약품 안전처. 2017.7. 보도자료)제제구분 유효성분 생산액
(원)바이오의약품 내
비중(%)국내시장규모
(비중)2015 2016 혈장분획제제 혈액을 원료로 하는 혈액분획제제 3,789 3,756 18.7 4,576억원 (25.7%) 혈액제제 혈액을 원료로 하는 혈액성분제제 2,333 2,198 11.0 세포치료제 체외에서 배양, 증식, 선별, 조작한 살아있는 세포 340 365 1.8 107억원
(0.1%)
국내는 물론 전세계적으로 수혈용 혈액이 부족하고 수혈 관련 부작용 및 일부 환자들에게 적절한 혈액을 구할 수 없는 문제점 등 때문에 인공혈액 개발이 시급하다(1). 줄기세포 유래 혈액 개발 관련해서는 영국, 일본, 미국, 네덜란드, 프랑스 등에서 활발히 연구가 진행되고 있다. 2000년대 중반부터 시작된 줄기세포기반의 혈액 생산 연구는 기존에 세포가 잘 배양됨을 보여주는 기초적인 연구에서 이제 임상시험과 대량생산이라는 새로운 시기로 접어들고 있다(1).
- 2. 줄기세포 유래 적혈구 제제의 첫 번째 임상시험
- 프랑스의 Douay 박사 연구팀은 2011년에 1명에게 자가 말초혈 백혈구 성분채집으로 얻은 CD34양성 세포로부터 적혈구를 1 mL 생산하여 최초로 인체 내 자가수혈하였다(2). 프랑스 Hospital Saint Antoine에서 시행된 이 연구에서는 수혈 후 한달 뒤에 다시 혈액을 채집해 줄기세포 유래 체외 생산 적혈구가 얼마나 남아있는지 검증하고자 하였으며, 체외 생산 혈액이 헌혈혈액만큼 오래 살 수 있으며 안전하다고 보여주었다.
그러나 다른 성체 줄기세포의 한계와 마찬가지로 제대혈이나 말초혈액으로부터 수혈용 적혈구를 생산하기에는 얻을 수 있는 최종 적혈구 수에 한계가 있다. 미국 Arteriocyte 회사가 미국 국방부 연구소로부터 지원받아 시행한 연구에서 제대혈 한 팩에서 10 unit을 만들 수 있다고 주장하기도 하였으나, 이는 이론적인 계산에 의한 것이며 실현된 바 없다.
적혈구 체외 생산이 다른 세포치료제제와 크게 다른 점 중 하나는, 치료에 필요한 세포수가 다른 세포치료제와 현격히 다르다는 것이다. 중간엽줄기세포와 같은 다른 세포치료제제는 1 dose 당 보통 106-108 개 정도 세포가 필요하지만, 적혈구 제제는 한 유닛(unit)에 2×1012개의 적혈구가 들어있으며 대량출혈의 경우 한 사람이 수 십개 유닛을 수혈받기도 하고, 주기적으로 계속적인 수혈이 필요하기도 하다. 따라서, 안전성이나 기능은 물론 경제적으로 생산할 수 있는지의 문제가 해결되어야 한다.
성체 줄기세포에서 바로 적혈구를 만들게 되면 처음 source에 있던 조혈모세포 수가 중요한데, 골수는 건강한 기증자를 얻기 힘들고, 제대혈인 경우는 공여자 간 variation이 크고, 이론과 달리 실제로 추출하면 한 단위에서 대개 2×106개 이하의 조혈모세포를 얻게 된다. 그리고 세포 증식의 한계 때문에, 이것으로 헌혈혈액 한 팩에 해당하는 양을 reproducible하게 생산하기는 현 기술로는 어려워 보인다. 그럼에도 불구하고, 유전자 주입 등을 통해 만든 줄기세포 유래 적혈구는 안전성 등 해결해야 할 난관들이 아직 많기 때문에, 적혈구 제제에 대해서는 아직은 성체줄기세포를 이용한 제제에 대해서만 임상시험이 진행중이다.
- 3. 줄기세포 유래 적혈구 제제의 두 번째 임상시험
- 영국에서는 성체줄기세포로부터 실험실에서 만든 적혈구를 2019에 시작을 목표로 ‘RESTORE (REcover and survival of STem cell Originated REd cells) clinical trial’ 로 불리는 ‘first-in-human clinical trial’을 진행중이다. David Anstee 교수와 Ashley Toye 교수가 책임자로 있는 NIHR (National Institute for Health Research) Blood and Transplant Research Units (BTRU)에서는 임상시험을 위해 지원자를 모집중이며 £12.1 million (약 181억)을 지원받았다. 이 임상시험은 2015년에 계획되어 2017년 내에 진행할 예정이었지만 지연되어 현재 진행중이다.
NHSBT Filton, Bristol 대학에서 세포를 만들고 Addenbrookes’ Hospital Cambridge 에서 임상시험을 시행한다. 이 임상시험은 선별된 혈액형을 가진 자발적 공여자로부터 조혈모세포를 기증받아 혈액을 생산하며, 20명의 임상시험 참가자는 첫번째에는 말초 혈액을 뽑아 바로 수혈 받고, 4개월 뒤에는 같은 공여자의 조혈모세포에서 만든 약 5mL 정도의 혈액을 수혈 받는 프로그램이다 연구진은 공여자에게서 뽑은 적혈구에 비해 실험실에서 만든 적혈구가 더 young 하기 때문에 체내에서 더 오래 살아남을 것이라고 예상하고 있다. 이 가설이 확인된다면, 앞으로 체외생산 적혈구는 현재 헌혈 혈액보다도 약 3분의 1 용량으로도 비슷한 효과를 유지할 수 있을 것이다. 그렇다면 기증된 제대혈 한 유닛에서 그 정도 양은 현재 기술로도 만들 수 있기 때문에 앞으로 계속 사용될 가능성이 높을 것이다.
실험실에서 만든 적혈구 제제는 주기적으로 수혈이 필요한 겸상적혈구빈혈 혹은 지중해빈혈 및 일부 암 환자들에게 안전하고 효율적인 수혈제제가 될 것이다. 이 혈액 제제는 헌혈혈액과 달리 매우 fresh해서, 수혈량을 줄일 수 있고, 빈번한 수혈로 인한 부작용(혈액량이 줄어들면 iron overload 같은 부작용이 생김)을 줄일 수 있어 성공한다면 헌혈혈액보다 매우 우수한 상품이 될 것으로 예상된다.
영국에서는 매해 150만 유닛의 적혈구 헌혈과 수혈이 이뤄지고 있는데, 이 연구는 혈액원에서 적절한 혈액을 구할 수 없는 희귀 혈액형을 가진 사람들로부터 줄기세포로부터 신선한 혈액을 만들어 피를 일부 뽑아 혈액을 만들어 수혈하게 하는 것으로서 성공한다면 그 가치가 매우 크다.
<체외 혈액 생산 방법>
Donation된 혈액에서 백혈구를 분리한다. 이 중에 포함된 적은 양의 줄기세포를 magnetic bead를 이용하여 분리한다. 이 세포를 약 3주간 영양분과 growth factor를 넣은 배지에서 배양한다. 세포들이 증식함에 따라 이 세포를 더 큰 bottle로 옮겨 나중에는 3L의 8개 bottle에 차게 된다. 이 안에 있는 성숙한 적혈구계 세포들을 필터하고 농축시키면1-2 teaspoon에 해당하는 체외생산 적혈구가 된다.

그림 1. 인큐베이터 안 바이오리액터 내에서 적혈구세포를 배양하고 잇는 모습
(그림 source: NHSBT).
- 4. 역분화줄기세포로부터 적혈구 생산 연구
- 역분화줄기세포를 만든 후 조혈모세포와 적혈구전구세포로 분화시켜 혈액을 만드는 연구도 최근 많이 진척되었다. 자가혈액으로부터 역분화줄기세포를 만드는 방법은, 적합한 혈액을 찾기 어려운 희귀혈액형 및 복합 항체를 가진 환자에게 유용할 것이다. 그러나 역분화줄기세포 유래 혈액의 경우 탈핵율이 매우 낮고 제대로 된 기능을 보이는 적혈구 생산까지는 아직 연구가 더 진척되어야 한다(3).
프랑스의 Douay 교수 연구팀은, 적혈구에 대한 항체를 지녀 특수혈액이 필요한 동종면역환자나 희귀혈액형을 가진 사람을 위해 3명의 역분화줄기세포주를 확보 만으로도 이런 환자의 99%까지 적합한 혈액 공급이 이론적으로 가능하다고 하였다(4). 프랑스의 희귀혈액형 보유 환자를 대상으로 할 때 15명의 O형 및 희귀혈액형을 갖는 정상인으로부터 역분화줄기세포를 제작할 수 있다면 거의 모든 사람들에게 적합한 혈액을 공급가능하며, 이는 대부분의 나라에 비슷하게 적용 가능하리라 생각된다.
- 5. 적혈구 전구세포주로부터 적혈구 생산 연구
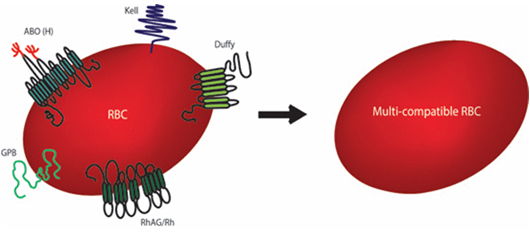
그림 2. 적혈구전구세포에서 gene editing으로 여러 혈액형 유전자를 제거하여 multi-compatible RBC를 만드는 모식도 (출처: 참고문헌 5)
영국 Bristol 대학의 Toye 교수팀은 2018년에 immortalised erythroblast에 CRISPR–Cas9을 이용해 여러 유전자를 동시에 제거하여 수혈시 문제될 수 있는 여러 항원들을 제거해 사실상 universal donor cell로 사용될 수 있는 적혈구를 만드는 데 성공했다. 5개 혈액형 그룹이 완전 음성인 표현형을 가지는 적혈구가 만들어졌다. 이렇게 만들어진 혈액은 완전히 성숙되기 전의 reticulocyte(망상적혈구)이지만 동물실험에서 체내에 들어가면 적혈구로 성숙됨을 보여줬고 어른 혈색소를 가지고 있으며, 여러 기능검사에서도 헌혈혈액과 비슷하여 매우 고무적인 결과를 보여줬다. 동물실험에서 세포주 유래 적혈구와 일반 헌혈혈액 간에 생존기간에 차이가 없었다.
- 6. 줄기세포 유래 혈소판 제제 첫번째 임상시험
- 에토 고지 교토대 교수가 2018년 8월에 일본 후생노동성의 허가를 받아, 유도만능줄기세포로 만든 인공 혈소판에 대한 임상시험 계획을 발표했다. 이는 줄기세포 유래 인공 혈소판에 대한 세계 최초의 임상시험이다. 대상자는 골수 조혈모세포 감소 및 생성문제로 혈액세포가 생성되지 않아 혈소판 수혈이 필요한 재생불량성빈혈 환자들이다. 6개월간 총 3회 수혈하여 1년간 효능과 안전성을 검증받게 된다. 유도만능줄기세포로 만든 혈액 성분의 경우로는 처음 실시되는 임상시험이 된다. Megakaryon 회사는 교토대학교에서 유도만능줄기세포를 제공받아 혈소판을 만들어내서 혈액제재를 제조하는 개발을 진행하고 있으며 향후 미국에서의 임상시험도 준비중이라고 발표했다.
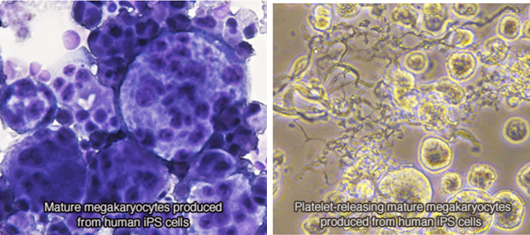
그림 3. (좌) 유도만능줄기세포로부터 만들어진 성숙한 megakaryocyte (거핵세포; 혈소판 전구세포)와 (우) 혈소판을 만들어내고 있는 사진. (자료출처: Megakaryon corporation 홈페이지)
- 7. 결론 및 향후 전망
- 곧 체외 생산 줄기세포 유래 적혈구 제제와 혈소판 제제의 임상시험이 개시될 것이고 전망은 밝은 편이다. 임상시험이 잘 끝난다면, 적합한 혈액이 없어 고통받는 환자들에게 큰 도움이 될 수 있을 것이다. 유도만능줄기세포나 세포주 유래 혈액 생산 연구가 더 진척되어 경제성까지 갖추게 되면, 기존의 헌혈자에 의존하던 혈액 공급 시스템이 많이 바뀌리라 예상된다.
- References
- 1. Choe WH, Baek EJ. Artificial blood: from the past to the future. ISBT Science Series 2015;10:150-153.
2. Giarratana MC, Rouard H, Dumont A, Kiger L, Safeukui I, Le Pennec PY, et al. Proof of principle for transfusion of in vitro-generated red blood cells. Blood. 2011;118:5071–5079.
3. Kim, S, Baek EJ. Cell sources for large-scale manufacture of red blood cells. ISBT science series 2018:13;268-273.
4. Peyrard T, Bardiaux L, Krause C, Kobari L, Lapillonne H, Andreu G, et al. Banking of pluripotent adult stem cells as an unlimited source for red blood cell production: potential applications for alloimmunized patients and rare blood challenges. Transfus Med Rev 2011;25:206-216.
5. Hawksworth J, Satchwell TJ, Meinders M, Daniels DE, Regan F, Thornton NM, et al. Enhancement of red blood cell transfusion compatibility using CRISPR‐mediated erythroblast gene. EMBO Mol Med. 2018;10:e8454.
